Электрический ток в жидкостях — теория, электролиз
«Физика – 10 класс»
Каковы носители электрического тока в вакууме?
Каков характер их движения?
Жидкости, как и твёрдые тела, могут быть диэлектриками, проводниками и полупроводниками. К диэлектрикам относится дистиллированная вода, к проводникам — растворы и расплавы электролитов: кислот, щелочей и солей. Жидкими полупроводниками являются расплавленный селен, расплавы сульфидов и др.
Электролитическая диссоциация.
При растворении электролитов под влиянием электрического поля полярных молекул воды происходит распад молекул электролитов на ионы.
Распад молекул на ионы под влиянием электрического поля полярных молекул воды называется электролитической диссоциацией.
Степень диссоциации — доля в растворённом веществе молекул, распавшихся на ионы.
Степень диссоциации зависит от температуры, концентрации раствора и электрических свойств растворителя.
С увеличением температуры степень диссоциации возрастает и, следовательно, увеличивается концентрация положительно и отрицательно заряженных ионов.
Ионы разных знаков при встрече могут снова объединиться в нейтральные молекулы.
При неизменных условиях в растворе устанавливается динамическое равновесие, при котором число молекул, распадающихся за секунду на ионы, равно числу пар ионов, которые за то же время вновь объединяются в нейтральные молекулы.
Ионная проводимость.
Носителями заряда в водных растворах или расплавах электролитов являются положительно и отрицательно заряженные ионы.
Если сосуд с раствором электролита включить в электрическую цепь, то отрицательные ионы начнут двигаться к положительному электроду — аноду, а положительные — к отрицательному — катоду. В результате по цепи пойдёт электрический ток.
Проводимость водных растворов или расплавов электролитов, которая осуществляется ионами, называют ионной проводимостью.
Жидкости могут обладать и электронной проводимостью. Такой проводимостью обладают, например, жидкие металлы.
Электролиз. При ионной проводимости прохождение тока связано с переносом вещества. На электродах происходит выделение веществ, входящих в состав электролитов. На аноде отрицательно заряженные ионы отдают свои лишние электроны (в химии это называется окислительной реакцией), а на катоде положительные ионы получают недостающие электроны (восстановительная реакция).
Жидкости могут обладать и электронной проводимостью. Такой проводимостью обладают, например, жидкие металлы.
Процесс выделения на электроде вещества, связанный с окислительновосстановительными реакциями, называют электролизом.
От чего зависит масса вещества, выделяющегося за определённое время? Очевидно, что масса m выделившегося вещества равна произведению массы m0i одного иона на число Ni ионов, достигших электрода за время Δt:
Масса иона m0i равна:

где М — молярная (или атомная) масса вещества, a NA — постоянная Авогадро, т. е. число ионов в одном моле.
Число ионов, достигших электрода, равно:

где Δq = IΔt — заряд, прошедший через электролит за время Δt; q0i — заряд иона, который определяется валентностью n атома: q0i = пе (е — элементарный заряд). При диссоциации молекул, например КВr, состоящих из одновалентных атомов (n = 1), возникают ионы К + и Вr – . Диссоциация молекул медного купороса ведёт к появлению двухзарядных ионов Си 2+ и SO 2- 4 (n = 2). Подставляя в формулу (16.3) выражения (16.4) и (16.5) и учитывая, что Δq = IΔt, a q0i = nе, получаем

Закон Фарадея.
Обозначим через k коэффициент пропорциональности между массой m вещества и зарядом Δq = IΔt, прошедшим через электролит:

где F = eNA = 9,65 • 10 4 Кл/моль — постоянная Фарадея.
Коэффициент k зависит от природы вещества (значений М и n). Согласно формуле (16.6) имеем
Закон электролиза Фарадея:
Масса вещества, выделившегося на электроде за время Δt. при прохождении электрического тока, пропорциональна силе тока и времени.
Это утверждение, полученное теоретически, впервые было установлено экспериментально Фарадеем.
Величину k в формуле (16.8) называют электрохимическим эквивалентом данного вещества и выражают в килограммах на кулон (кг/Кл).
Из формулы (16.8) видно, что коэффициент к численно равен массе вещества, выделившегося на электродах, при переносе ионами заряда, равного 1 Кл.

Электрохимический эквивалент имеет простой физический смысл. Так как M/NA = m0i и еn = q0i, то согласно формуле (16.7) k = rn0i/q0i, т. е. k — отношение массы иона к его заряду.
Измеряя величины m и Δq, можно определить электрохимические эквиваленты различных веществ.
Убедиться в справедливости закона Фарадея можно на опыте. Соберём установку, показанную на рисунке (16.25). Все три электролитические ванны заполнены одним и тем же раствором электролита, но токи, проходящие через них, различны. Обозначим силы токов через I1, I2, I3. Тогда I1 = I2 + I3. Измеряя массы m1, m2, m3 веществ, выделившихся на электродах в разных ваннах, можно убедиться, что они пропорциональны соответствующим силам токов I1, I2, I3.
Определение заряда электрона.
Формулу (16.6) для массы выделившегося на электроде вещества можно использовать для определения заряда электрона. Из этой формулы вытекает, что модуль заряда электрона равен:

Зная массу m выделившегося вещества при прохождении заряда IΔt, молярную массу М, валентность п атомов и постоянную Авогадро NA, можно найти значение модуля заряда электрона. Оно оказывается равным e = 1,6 • 10 -19 Кл.
Именно таким путём и было впервые в 1874 г. получено значение элементарного электрического заряда.
Применение электролиза. Электролиз широко применяют в технике для различных целей. Электролитическим способом покрывают поверхность одного металла тонким слоем другого (никелирование, хромирование, позолота и т. п.). Это прочное покрытие защищает поверхность от коррозии. Если обеспечить хорошее отслаивание электролитического покрытия от поверхности, на которую осаждается металл (этого достигают, например, нанося на поверхность графит), то можно получить копию с рельефной поверхности.
Процесс получения отслаиваемых покрытий — гальванопластика — был разработан русским учёным Б. С. Якоби (1801—1874), который в 1836 г. применил этот способ для изготовления полых фигур для Исаакиевского собора в Санкт-Петербурге.
Раньше в полиграфической промышленности копии с рельефной поверхности (стереотипы) получали с матриц (оттиск набора на пластичном материале), для чего осаждали на матрицы толстый слой железа или другого вещества. Это позволяло воспроизвести набор в нужном количестве экземпляров.
При помощи электролиза осуществляют очистку металлов от примесей. Так, полученную из руды неочищенную медь отливают в форме толстых листов, которые затем помещают в ванну в качестве анодов. При электролизе медь анода растворяется, примеси, содержащие ценные и редкие металлы, выпадают на дно, а на катоде оседает чистая медь.
При помощи электролиза получают алюминий из расплава бокситов. Именно этот способ получения алюминия сделал его дешёвым и наряду с железом самым распространённым в технике и быту.
С помощью электролиза получают электронные платы, служащие основой всех электронных изделий. На диэлектрик наклеивают тонкую медную пластину, на которую наносят особой краской сложную картину соединяющих проводов. Затем пластину помещают в электролит, где вытравливаются не закрытые краской участки медного слоя. После этого краска смывается, и на плате появляются детали микросхемы.
Источник: «Физика – 10 класс», 2014, учебник Мякишев, Буховцев, Сотский
Электрический ток в различных средах – Физика, учебник для 10 класса – Класс!ная физика
Электрический ток в жидкостях — теория, электролиз
То, что жидкости могут отлично проводить электрическую энергию, знают абсолютно все. И также общеизвестным фактом является то, что все проводники по своему типу делятся на несколько подгрупп. Предлагаем рассмотреть в нашей статье, как электрический ток в жидкостях, металлах и прочих полупроводниках проводится, а также законы электролиза и его виды.
Теория электролиза
Чтобы было легче понять, о чем идет речь, предлагаем начать с теории, электричество, если мы рассматриваем электрический заряд, как своего рода жидкость, стало известным уже более 200 лет. Заряды состоят из отдельных электронов, но те, настолько малы, что любой большой заряд ведет себя как непрерывного течения, жидкость.
Как и тела твердого типа, жидкие проводники могут быть трех типов:
- полупроводниками (селен, сульфиды и прочие);
- диэлектиками (щелочные растворы, соли и кислоты);
- проводниками (скажем, в плазме).
Процесс, при котором происходит растворение электролитов и распадение ионов под воздействием электрического молярного поля, называется диссоциация. В свою очередь, доля молекул, которые распались на ионы, либо распавшихся ионов в растворенном веществе, полностью зависит от физических свойств и температуры в различных проводниках и расплавах. Обязательно нужно помнить, что ионы могут рекомбинироваться или вновь объединиться. Если условия не будут меняться, то количество распавшихся ионов и объединившихся будет равно пропорциональным.
В электролитах проводят энергию ионы, т.к. они могут являться и положительно заряженными частицами, и отрицательно. Во время подключения жидкости (или точнее, сосуда с жидкостью к сети питания), начнется движение частиц к противоположным зарядам (положительные ионы начнут притягиваться к катодам, а отрицательные – к анодам). В этом случае, энергию транспортируют непосредственно, ионы, поэтому проводимость такого типа называется – ионной.
Во время этого типа проводимости, ток переносят ионы, и на электродах выделяются вещества, которые являются составляющими электролитов. Если рассуждать с точки зрения химии, то происходит окисление и восстановление. Таким образом, электрический ток в газах и жидкостях транспортируется при помощи электролиза.
Законы физики и ток в жидкостях
Электричество в наших домах и технике, как правило, не передается в металлических проволоках,. В металле электроны могут переходить от атома к атому, и, таким образом нести отрицательный заряд.
Как жидкости, они приводятся в виде электрического напряжения, известного как напряжение, изменяемом в единицах – вольт, в честь итальянского ученого Алессандро Вольта.
Также, электрический ток течет от высокого напряжения в низкое напряжение и измеряется в единицах, известных как ампер, названных по имени Андре-Мари Ампера. И согласно теории и формулы, если увеличить напряжение тока, то его сила также увеличится пропорционально. Это соотношение известно как закон Ома. Как пример, виртуальная ампермерная характеристика ниже.
 Рисунок: зависимость тока от напряжения
Рисунок: зависимость тока от напряжения
Закон Ома (с дополнительными подробностями относительно длины и толщины проволоки), как правило, является одним из первых вещей, преподаваемых в классах, изучающих физику, многие студенты и преподаватели поэтому рассматривают электрический ток в газах и жидкостях как основной закон в физике.
Для того чтобы увидеть своими глазами движение зарядов, нужно приготовить колбу с соленой водой, плоские прямоугольные электроды и источники питания, также понадобится ампермерная установка, при помощи которой будет проводиться энергия от сети питания к электродам.
 Рисунок: Ток и соль
Рисунок: Ток и соль
Пластины, которые выступают проводниками необходимо опустить в жидкость, и включить напряжение. После этого начнется хаотичное перемещение частиц, но как после возникновения магнитного поля между проводниками, этот процесс упорядочится.
Как только ионы начнут меняться зарядами и объединяться, аноды станут катодами, а катоды – анодами. Но здесь нужно учитывать и электрическое сопротивление. Конечно, не последнюю роль играет теоретическая кривая, но основное влияние – это температура и уровень диссоциации (зависит от того, какие носители будут выбраны), а также выбран переменный ток или постоянный. Завершая это опытное исследование, Вы можете обратить внимание, что на твердых телах (металлических пластинах), образовался тончайший слой соли.
Электролиз и вакуум
Электрический ток в вакууме и жидкостях – это достаточно сложный вопрос. Дело в том, что в таких средах полностью отсутствуют заряды в телах, а значит, это диэлектрик. Иными словами, наша цель – это создание условий, для того, чтобы атом электрона мог начать свое движение.
Для того нужно использовать модульное устройство, проводники и металлические пластины, а далее действовать, как и в методе выше.
 Проводники и вакуум
Проводники и вакуум  Характеристика тока в вакууме
Характеристика тока в вакууме
Применение электролиза
Этот процесс применяется практически во всех сферах жизни. Даже самые элементарные работы подчас требуют вмешательства электрического тока в жидкостях, скажем,
При помощи этого простого процесса происходит покрытие твердых тел тончайшим слоем какого-либо металла, например, никелирование иди хромирование Т.е. это один из возможных способов борьбы с коррозийными процессами. Подобные технологии используются в изготовлении трансформаторов, счетчиков и прочих электрических приборов.
Надеемся, наше обоснование ответило на все вопросы, которые возникают, изучая явление электрический ток в жидкостях. Если нужны более качественные ответы, то советуем посетить форум электриков, там Вас с радостью проконсультируют бесплатно.
Физика. 10 класс
Электролиз
Электрический ток в жидкостях
Необходимо запомнить
Жидкости по степени электропроводности делятся на:
– диэлектрики (дистиллированная вода);
– полупроводники (расплавленный селен).
Электролит – это проводящая электрический ток жидкость (растворы кислот, щелочей, солей и расплавленные соли).
Электролитическая диссоциация – распад молекул электролита на ионы при растворении в воде или расплавлении.
Степень диссоциации – отношение числа молекул, распавшихся на ионы, к общему числу молекул, растворённого вещества. Степень диссоциации измеряется в долях или процентах.
Электропроводимость электролитов – ионная. Прохождение электрического тока связано с переносом вещества.
Явление электролиза – это выделение на электродах веществ, входящих в электролиты, в процессе окислительно-восстановительных реакций, которое возникает при прохождении через электролиты электрического тока.
Закон электролиза:
$m = m_0 cdot N = frac
$m = k cdot I cdot t$
Закон электролиза определяет массу вещества, выделяемого на электроде при электролизе за время прохождения электрического тока.
k – электрохимический эквивалент вещества, численно равный массе вещества, выделившегося на электроде при прохождении через электролит заряда в 1 Кл.
m – масса выделившегося вещества,
NA – число Авогадро,
M – молярная масса,
I – сила тока,
e – заряд электрона,
n – число ионов.
Применение электролиза:
– получение чистых металлов (очистка от примесей);
– гальваностегия (никелирование, хромирование и т. д.);
– гальванопластика, т. е. получение отслаиваемых покрытий (рельефных копий).
Лабораторная работа «Определение элементарного заряда методом электролиза»
Техническое применения электролиза
Гальваностегия – покрытие металлических изделий тонким слоем другого металла (никелирование, хромирование, серебрение, золочение и т. д.) с целью предохранения от окисления и придания изделию привлекательного внешнего вида. Предмет, подлежащий покрытию, тщательно очищают, хорошо обезжиривают и помещают в качестве катода в электролитическую ванну, содержащую раствор соли того металла, которым должен быть покрыт данный предмет. Анодом служит пластинка из того же металла. Для более равномерного покрытия обычно применяют две пластинки в качестве анода, помещая предмет между ними.
Гальванопластика – электролитическое изготовление копий с рельефных предметов (медалей, гравюр, барельефов и т. д.). С рельефного предмета делают восковый или иной слепок. Затем поверхность слепка покрывают тонким слоем графита, чтобы она стала проводящей. В таком виде слепок используется в качестве катода, который опускают в электролитическую ванну с раствором медного купороса. Анодом служит медная пластинка. Когда на слепке нарастет достаточно толстый слой меди, электролиз прекращают и воск осторожно удаляют. Остается точная медная копия оригинала.
В полиграфической промышленности такие копии (стереотипы) получают с оттиска набора на пластичном материале (матрица), осаждая на матрицах толстый слой железа или другого материала. Это позволяет воспроизвести набор в нужном количестве экземпляров. Если раньше тираж книги ограничивался числом оттисков, которые можно получить с одного набора (при печатании набор стирается), то использование стереотипов позволяет значительно увеличить тираж.
Правда, в настоящее время с помощью электролиза получают стереотипы только для книг высококачественной печати и с большим числом иллюстраций.
Осаждая металл на длинный цилиндр, получают трубы без шва.
Процесс получения отслаиваемых покрытий был разработан русским учёным Якоби Б.С., который в 1836 г. применил этот способ для изготовления полых фигур для Исаакиевского собора (в Санкт-Петербурге).
Рафинирование меди
Медь является лучшим материалом для изготовления проводников, но для этого она должна быть лишена каких бы то ни было примесей. Очищение меди от примесей называется рафинированием (очисткой) меди. Массивные куски (толстые листы) неочищенной меди, полученной при выплавке из руды, являются анодом, а тонкие пластинки из чистой меди – катодом. Процесс происходит в больших ваннах с водным раствором медного купороса. При электролизе медь анода растворяется; примеси, содержащие ценные и редкие металлы, выпадают на дно в виде осадка (шлама), а на катоде оседает чистая медь. Таким же образом производят рафинирование некоторых других металлов.
Получение алюминия
При помощи электролиза получают алюминий. Для этого подвергают электролизу не растворы солей этого металла, а его расплавленные оксиды.
В угольные тигли насыпают глинозём (оксид алюминия Аl2O3), полученный путем переработки бокситов – руд, содержащих алюминий. Тигель служит катодом. Анодом являются угольные стержни, вставленные в тигель. Сначала угольные стержни опускают до соединения с тиглем и пропускают сильный ток. Глинозём при прохождении тока нагревается и расплавляется. После этого угли поднимают, ток проходит через жидкость и производит электролиз. Расплавленный алюминий, выделяющийся при электролизе, опускается на дно тигля (катод), откуда его через особое отверстие выпускают в формы для отливки.
Описанный способ получения алюминия сделал его дешевым и наряду с железом самым распространенным в технике и быту металлом.
Путем электролиза расплавленных солей в настоящее время получают также натрий, калий, магний, кальций и другие металлы.
Электролиз используется для гальваностегии, гальванопластики, рафинирования меди, получения алюминия и других целей.
Электрический ток в жидкостях
Знакомство с явлением
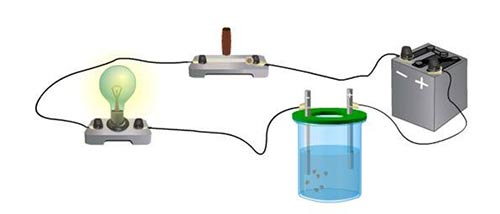
Соединим с источником тока последовательно лампу и электролитическую ванну с дистиллированной водой, в которую опущены угольные электроды. Химически чистая вода почти не проводит ток.

Если же в воде растворить соль (например CuSO4, CuCl2), то лампочка загорится, а на катоде из раствора выделится медь.
Электролитическая диссоциация
По способности проводить электрический ток в водном растворе и расплаве все вещества делятся на электролиты и неэлектролиты.
Электролитическая диссоциация – явление расщепления нейтральных молекул кислот, солей и щелочей при их растворении на положительные и отрицательные ионы.
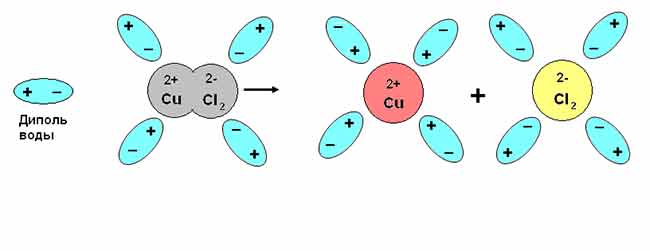
Интенсивность электролитической диссоциации зависит:
- От температуры раствора.
- От концентрации раствора.
- От рода раствора (его диэлектрической проницаемости).
Электрический ток в растворах и (или расплавах) электролитов представляет собой упорядоченное перемещение ионов обоих знаков в противоположных направлениях.
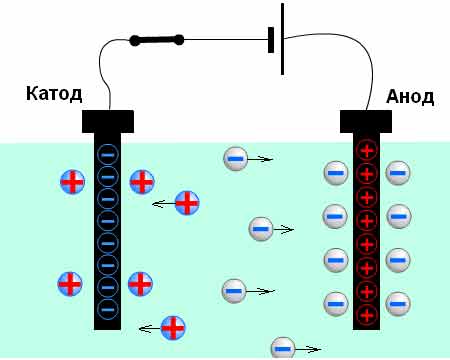
На вольт-амперной характеристике график смещен вследствие явления поляризации.
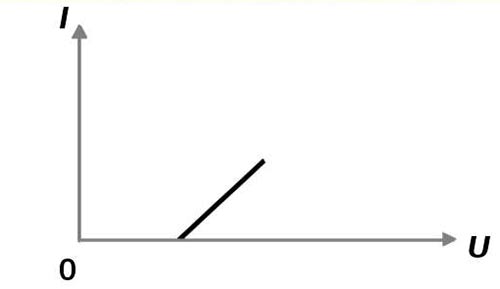
Справедлив закон Ома при неизменной концентрации раствора и температуры.
Электролиз
Электролиз – перенос вещества при прохождении электрического тока через электролит.
Электролиз сопровождается выделением на электродах, опущенных в электролит, составных частей растворенного вещества.
Закон электролиза Фарадея
Масса вещества, выделившегося на электроде за время Dt при прохождении электрического тока, пропорциональна силе тока и времени:

k – электрохимический эквивалент вещества (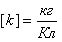 ).
).
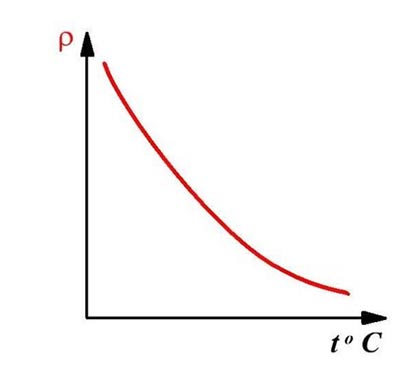
Сопротивление электролита уменьшается с ростом температуры, т. к. увеличивается количество ионов вследствие электролитической диссоциации.
Закон Фарадея позволяет определить заряд электрона:
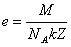
Вывод о существовании в природе элементарного электрического заряда был сделан Гельмгольцем в 1881 г.
Применение электролиза
Рафинирование (очистка) металлов
Процесс происходит в электролитической ванне. Анодом служит металл, подлежащий очистке, катодом – тонкая пластинка из чистого металла, а электролитом – раствор соли данного металла, например при рафинировании меди – раствор медного купороса.
При определенных условиях на катоде выделяется чистая медь, а примеси выпадают в виде осадка или переходят в раствор.

Электрометаллургия
Некоторые металлы, например алюминий, получают методом электролиза из расплавленной руды. Электролитической ванной и одновременно катодом служит железный ящик с угольным подом, а анодом – угольные стержни. Температура руды (около 900 0 С) поддерживается протекающим в ней током. Расплавленный алюминий опускается на дно ящика, откуда его через отверстие выпускают в форму для отливки.

Гальваностегия
Электролитический способ покрытия металлических изделий слоем благородных металлов не поддающихся окислению.

Гальванопластика
Используется для воспроизведения формы рельефных предметов (медалей, монет, точных копий художественных изделий).

Электроэпиляция
Используется в косметологии для удаления волос воздействием на волосяные фолликулы очень тонкими иголками.
Электрический ток в жидкостях. Закон электролиза
Урок 79. Физика 10 класс


В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности



Конспект урока “Электрический ток в жидкостях. Закон электролиза”
Как и другие тела, жидкости могут являться проводниками, полупроводниками и диэлектриками. Например, дистиллированная вода является диэлектриком. Это легко подтверждается с помощью опыта. Поместим два электрода в ванну с водой. Эти электроды мы подсоединим к источнику тока, а также включим в цепь лампочку и выключатель. Как и всегда, с помощью выключателя мы можем замыкать и размыкать цепь, ну а лампочка будет служить индикатором того, что по цепи протекает электрический ток.

Итак, если мы замкнем цепь, то никакого электрического тока мы не получим: ведь дистиллированная вода является диэлектриком. Разомкнем цепь и насыплем в ванну некоторое количество самой обычной поваренной соли. Подождав, пока соль растворится, снова замкнем цепь. В этом случае, лампочка загорится, что будет означать протекание электрического тока по всей цепи. Давайте разберемся, как же соль могла повлиять на проводимость воды.
После того, как мы насыпали соль в ванну, там образовался солевой раствор. Как вы знаете из курса химии, молекулы воды являются полярными, так же, как и молекулы поваренной соли. Центр распределения положительного заряда в поваренной соли приходится на ион натрия, а центр распределения отрицательного заряда приходится на ион хлора. В результате, молекулы воды ориентируются таким образом, что вокруг иона натрия скапливаются отрицательные полюса молекул воды, а вокруг иона хлора — скапливаются положительные полюса молекул воды.
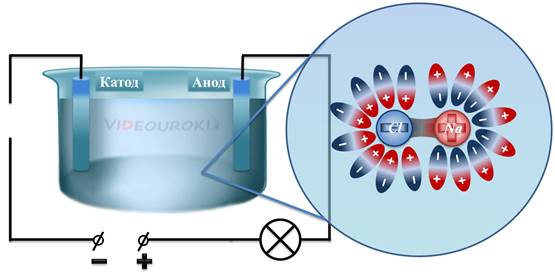
В этом случае, действие кулоновских сил достаточно велико, чтобы расщепить молекулу поваренной соли. То есть, молекула распадается на ион натрия и ион хлора.
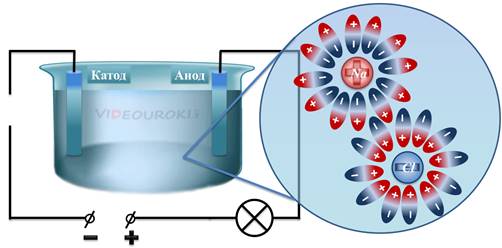
Таким образом, в растворе возникают заряженные частицы — ионы. В результате, отрицательные ионы (в данном случае ионы хлора), начинают двигаться к аноду, а положительные ионы (в данном случае ионы натрия) начинают двигаться к катоду. Это есть не что иное, как упорядоченное движение заряженных частиц, то есть электрический ток.
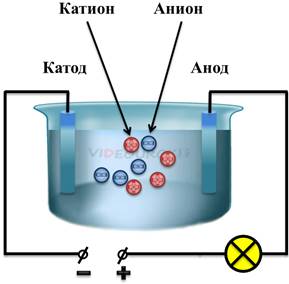
Процесс расщепления молекулы на ионы называется электролитической диссоциацией. То есть при электролитической диссоциации полярные молекулы распадаются под влиянием кулоновских сил. После распада молекулы, положительные ионы электролитов называются катионами, а отрицательные — анионами. Конечно, не все молекулы распадаются. Процент распавшихся молекул будет зависеть от концентрации раствора, температуры и, конечно, свойств самого электролита.
Таким образом, в водных растворах и расплавах электролитов возникает ионная проводимость. То есть, ионная проводимость — это проводимость, возникающая в результате переноса электрического заряда ионами. С ионной проводимостью связано понятие электролиза. Электролиз — это процесс выделения вещества на электроде в результате окислительно-восстановительных реакций.
Изучением данных вопросов активно занимался уже известный нам ученый Майкл Фарадей. Именно Фарадей впервые ввел такие термины, как электролиты, катионы и анионы, катод и анод.
Фарадей задался вопросом о том, как вычислить массу вещества, выделившегося на электроде в результате протекания электрического тока через электролит. Эту массу можно вычислить:
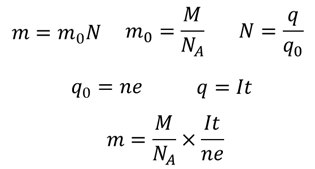
Именно к такому выводу и пришел Фарадей, установив, что масса вещества, выделившегося на электроде прямо пропорциональна силе тока, протекающего через электролит и времени протекания тока. Этот закон получил название закона Фарадея или закона электролиза. Как мы видим, в формуле есть несколько констант, которые было решено заменить на одну константу: = . Эта константа называется электрохимическим эквивалентом.
Если мы выразим электрохимический эквивалент из формулы, описывающей закон электролиза, то убедимся, что он измеряется в килограммах на кулон:
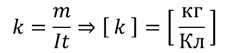
Иногда электрохимический эквивалент разделяют на две константы: число Фарадея (равного произведению элементарного заряда и числа Авогадро) и химический эквивалент (равный отношению молярной массы вещества к его валентности):
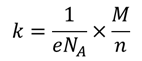
Электрохимические эквиваленты сведены в таблицы:
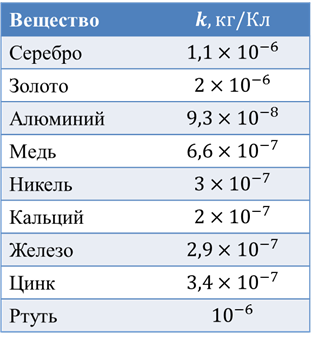
Но, даже если у вас нет этой таблицы, вы все равно сможете вычислить электрохимический эквивалент любого элемента, используя таблицу Менделеева. Для примера возьмем серебро:
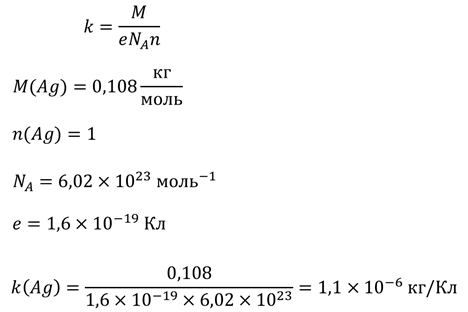
Кстати говоря, закон электролиза можно использовать, для экспериментального определения заряда электрона. Силу тока, протекающего через электролит, мы можем измерить, так же как и время протекания тока. Массу выделившегося на электроде вещества измерить тоже несложно. Таким образом, закон электролиза позволяет определить элементарный заряд:
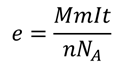
Электролиз широко используется в промышленности. Например, он используется для очистки металлов от примести, или, наоборот, для покрытия поверхности каким-то металлом. Такие процессы, как никелирование, хромирование, оцинковка или омеднение осуществляются благодаря открытию электролиза.
Пример решения задачи.
Задача. Для никелирования детали площадью 0,3 м 2 , на деталь требуется нанести слой толщиной 0,08 мм. Плотность никеля равна 8900 кг/м 3 . Какой ток нужно пустить через электролитическую ванну, чтобы полностью закончить никелирование за 3 часа?
Электрический ток в жидкостях
Каждый когда-то слышал определение электрического тока. Данное определение изображается как ориентированное перемещение заряженных частиц. Аналогичное перемещение в разных средах обладает принципиальными различиями. Как ключевой образец данного процесса возможно показать протекание и самораспространение электрического тока в жидкостных веществах.

Данные процессы квалифицируются разнообразными характеристиками и обладают серьёзными отличиями от целенаправленного перемещения заряженных частиц, происходящего в обыкновенных условиях не под влиянием разнообразных жидкостных веществ.
Формирование электрического тока в жидкостных веществах
Невзирая на то, что явление электропроводимости выполняется в основном благодаря проводникам из металла и их сплавов, электрический ток зависит от перемещения заряженных ионов, которые обрели либо, утратили по какой-то определённой причине необходимые атомные и молекулярные связи. Результатом данного перемещения является преобразование характеристик определённого вещества, где присутствуют ионы.
Следовательно, необходимо основываться на ключевую формулировку электрического тока, чтоб определить индивидуальное понимание образования электрического тока в разнообразных жидкостных веществах. Установлено, что разделение отрицательно заряженных ионов предоставляет поддержку перемещения в сферу источника электрического тока с положительными величинами. Положительно заряженные ионы в данных явлениях имеют возможность перемещаться в обратной ориентации – к отрицательному источнику электрического тока. Жидкостные проводники подразделяются на 3 ключевые вида:
- Полупроводники. Это расплавы сульфидов, а также расплавленный селен.
- Диэлектрики. К данному виду относятся: дистиллированная вода, керосин, растворы сахара, спирта, глюкозы.
- Проводники. К ним относятся растворы кислот, щелочей и солей.
Возможно определить, что электрический ток в жидкостных веществах способен появляться после преобразования состава и химических характеристик применяемых жидкостей. Это говорит полностью о противоположном по отношению к теории распределения электротока другими методами при применении обыкновенного проводника из металла.
Опыты Фарадея и электролиз
Протекание электротока в жидкостных веществах является продуктом движения заряженных ионов. Проблемные вопросы, которые связаны с появлением и распределением электрического тока в жидкостных веществах, явились основанием для исследований известного английского учёного, физика-экспериментатора и химика Майкла Фарадея. Майкл Фарадей благодаря множественным опытам на практике сумел отыскать свидетельства, что вес вещества, выделяемый в ходе электролиза, находится в зависимости от времени и электричества.
Сложно разобраться самому?
Попробуй обратиться за помощью к преподавателям
В то же время огромное значение имеет то, насколько длительно осуществляются эксперименты. В том числе, учёный сумел прояснить вопрос, что в ходе электролиза при отделении определённого вещества требуется одинаковое число электрических зарядов. Данное число получилось чётко определить и зарегистрировать в константе, получившая наименование числа Фарадея. В жидкостных веществах электроток обладает другими условиями распределения.
Электрический ток осуществляет взаимодействие с молекулярными соединениями воды. Молекулы воды в существенной мере производят затруднения всех перемещений ионов, а это не просматривалось в экспериментах с применением обыкновенного проводника из металла. Таким образом, формирование электрического тока при электролитических реакциях будет не настолько большим. Но с повышением температурных параметров жидкостного вещества проводимость со временем начинает повышаться. Это значит, что напряжение электротока возрастает.
В том числе, в ходе электролиза отмечалось, что вероятность распада определённой молекулы на отрицательные или положительные заряды ионов повышается из-за большого количества молекул применяемой жидкости. При насыщаемости жидкости ионами свыше определённых нормативов, осуществляется противоположный процесс. Проводимость жидкостного вещества снова становиться ниже.
Сегодня процесс электролиза нашёл своё использование в большинстве отраслей жизнедеятельности, а также в научной среде и в производственных процессах. Организации промышленности электролиз применяют в производстве и обрабатывании металла и металлических сплавов. Электрохимические реакции принимают участие в:
- Полировании плоскостей.
- Электролизе солей.
- Гальванике.
- Других окислительных и восстановительных работах.
Не нашли что искали?
Просто напиши и мы поможем
Электроток в вакууме и жидкостных веществах
Распространение электротока в жидкостных веществах и других средах является достаточно непростым процессом. Данный процесс обладает своими характеристиками, а также спецификой и свойствами. В аналогичных средах, как правило, в полной мере не содержатся заряды в объектах. По этой причине, данные вещества принято именовать диэлектриками.

Ключевой задачей исследовательских экспериментов было то, чтоб организовать такие условия, при которых атомы и молекулы смогли бы осуществлять собственное перемещение и процесс появления электротока начал бы осуществляться. Для осуществления таких исследовательских экспериментов традиционно применяются специализированная аппаратура и механизмы.
Ключевыми компонентами данных механизмов являются проводники в виде пластин из металла. Для установления главных показателей электрического тока требуется применить общеизвестные теории и уравнения. Одним из самых популярных считается закон Ома. Данный закон является универсальной токовой характеристикой. Здесь выполняется принципиальная зависимость электрического тока от напряжения.
Для осуществления экспериментов с водно-солевым веществом требуется подготовка сосуда, который будет содержать данный раствор, что придаст представление на практике процессам, происходящим при формировании электротока в жидкостных веществах. В том числе, установка обязана иметь электроды по типу прямоугольника, а также источники питания.
Для полнофункционального осуществления экспериментов необходимо обладать амперной установкой. Данная установка предоставить возможность осуществить электропитание электродов. В качестве электрических проводников являются пластины из металла. Металлические пластины окунаются в исследуемое жидкостное вещество, и после этого происходит подключение напряжения. Моментально осуществляется движение частиц.
Данное перемещение осуществляется в хаотичном порядке. При появлении магнитного поля меж электрическими проводниками все процессы перемещения элементов приходят в надлежащий порядок. Ионы осуществляют обмен зарядами, а также объединяются. Следовательно, катоды становятся анодами, а аноды становятся катодами. В данном процессе следует, в том числе, учесть ещё некоторое количество важнейших факторов:
- Температурные параметры.
- Электросопротивление.
- Уровень диссоциации.
- Применение переменного либо постоянного электротока.
По окончанию экспериментальных исследований осуществляется формирование пласта соли на металлических пластинах.
Электрический ток в жидкостях
Вы будете перенаправлены на Автор24
Всем знакомо определение электрического тока. Оно представляется как направленное движение заряженных частиц. Подобное движение в различных средах имеет принципиальные отличия. Как основной пример этого явления можно представить течение и распространение электрического тока в жидкостях. Такие явления характеризуются различными свойствами и серьезно отличаются от упорядоченного движения заряженных частиц, которое происходит в обычных условиях не под воздействием различных жидкостей.
Рисунок 1. Электрический ток в жидкостях. Автор24 — интернет-биржа студенческих работ
Формирование электрического тока в жидкостях
Несмотря на то, что процесс проводимости электрического тока осуществляется посредством металлических приборов (проводников), ток в жидкостях лежит в зависимости от движения заряженных ионов, которые приобрели или потеряли по некой определенной причине подобные атомы и молекулы. Показателем такого движения выступает изменение свойств определенного вещества, где проходят ионы. Таким образом, нужно опираться на основное определение электрического тока, чтобы сформировать специфическое понятие формирования тока в различных жидкостях. Определено, что разложение отрицательно заряженных ионов способствует движению в область источника тока с положительными значениями. Положительно заряженные ионы в таких процессах будут двигаться в противоположном направлении – к отрицательному источнику тока.
Жидкие проводники делятся на три основных типа:
- полупроводники;
- диэлектрики;
- проводники.
Электролитическая диссоциация – процесс разложения молекул определенного раствора на отрицательные и положительные заряженные ионы.
Готовые работы на аналогичную тему
Можно установить, что электроток в жидкостях может возникать после изменения состава и химического свойства используемых жидкостей. Это напрочь противоречит теории распространения электрического тока иными способами при использовании обычного металлического проводника.
Опыты Фарадея и электролиз
Течение электрического тока в жидкостях – это продукт процесса перемещения заряженных ионов. Проблемы, связанные с возникновение и распространением электротока в жидкостях, стали причиной изучения знаменитого ученого Майкла Фарадея. Он при помощи многочисленных практических исследований смог найти доказательства, что масса вещества, выделяемая в процессе электролиза, зависит от количества времени и электричества. При этом имеет значение время, в течение которого проводились эксперименты.
Также ученый смог выяснить, что в процессе электролиза при выделении определенного количества вещества необходимо одинаковое количество электрических зарядов. Это количество удалось точно установить и зафиксировать в постоянной величине, которая получила название числа Фарадея.
В жидкостях электрический ток имеет иные условия распространения. Он взаимодействует с молекулами воды. Они в значительной степени затрудняют все передвижения ионов, что не наблюдалось в опытах с использование обычного металлического проводника. Из этого следует, что образование тока при электролитических реакциях будет не столь большим. Однако при увеличении температуры раствора проводимость постепенно увеличивается. Это означает, что напряжение электрического тока растет. Также в процессе электролиза было замечено, что вероятность распада определенной молекулы на отрицательные или положительные заряды ионов увеличивается из-за большого числа молекул используемого вещества или растворителя. При насыщении раствора ионами сверх определенной нормы, происходит обратный процесс. Проводимость раствора вновь начинает снижаться.
В настоящее время процесс электролиза нашел свое применения во многих областях и сферах науки и на производстве. Промышленные предприятия его используют при получении или обработке металла. Электрохимические реакции участвуют в:
- электролизе солей;
- гальванике;
- полировке поверхностей;
- иных окислительно-восстановительных процессах.
Электрический ток в вакууме и жидкостях
Рисунок 2. Виды жидкостей. Автор24 — интернет-биржа студенческих работ
Распространение электрического тока в жидкостях и иных средах представляет собой довольно сложный процесс, который имеет собственные характеристики, особенности и свойства. Дело в том, что в подобных средах полностью отсутствуют заряды в телах, поэтому их принято называть диэлектриками. Главной целью исследований стало то, чтобы создать такие условия, при которых атомы и молекулы могли бы начать свое движения и процесс образования электрического тока начался. Для этого принято использовать специальные механизмы или устройства. Основным элементом таких модульных устройств стали проводники в виде металлических пластин.
Для определения основных параметров тока необходимо воспользоваться известными теориями и формулами. Самым распространенным являются закон Ома. Он выступает в роли универсальной амперной характеристики, где осуществляется принцип зависимости тока от напряжения. Напомним, что напряжение измеряется в единице Ампер.
Для проведения опытов с водой и солью необходимо подготовить сосуд с соленой водой. Это даст практическое и визуальное представление о процессах, которые происходят при образовании электрического тока в жидкостях. Также установка должна содержать электроды прямоугольной формы и источники питания. Для полномасштабной подготовки к опытам нужно иметь амперную установку. Она поможет провести энергию от сети питания к электродам.
В роли проводников будут выступать металлические пластины. Их опускают в используемую жидкость, а затем подключается напряжение. Сразу начинается перемещение частиц. Оно проходит в хаотичном режиме. При возникновении магнитного поля между проводниками все процессе движения частиц упорядочиваются.
Ионы начинают меняться зарядами и объединяться. Таким образом, катоды становятся анодами, а аноды – катодами. В этом процессе необходимо также учитывать еще несколько важных факторов:
- уровень диссоциации;
- температура;
- электрическое сопротивление;
- использование переменного или постоянного тока.
В конце эксперимента происходит образование слоя соли на пластинах.





